Получение муллита: фазовые трансформации каолинита, термодинамика процесса
- 1 — д-р геол.-минерал. наук главный научный сотрудник Институт геологии Коми научного центра Уральского отделения РАН ▪ Orcid
- 2 — канд. физ.-мат. наук старший научный сотрудник Сыктывкарский государственный университет им. Питирима Сорокина ▪ Orcid
- 3 — док. наук профессор Институт неметаллических полезных ископаемых ▪ Orcid
- 4 — младший научный сотрудник Институт геологии Коми научного центра Уральского отделения РАН ▪ Orcid
Аннотация
Рост потребности в муллитовом сырье, соответствующем промышленным требованиям, инициирует поиск его новых и альтернативных источников, а также эффективных технологий получения целевых продуктов (нанокомпозитов). В статье апробирован метод получения муллита из каолинита экспериментальным путем (Вежаю-Ворыквинское месторождение, Россия). Изучены структурные преобразования каолинита (системы Al-Si-O-Me), трансформации минеральных фаз и термодинамика процесса. На основе оценки термодинамики протекания реакций определена предпочтительная реакция образования муллита. Показано, что образование целевого продукта – муллитового нанокомпозита – имеет ряд промежуточных фаз (метакаолинит, псевдомуллит). Преобразования структуры исходного каолинита включают удаление структурной воды с разделением кремнекислородного тетраэдрического и алюмокислородного октаэдрического слоев, распад на свободные оксиды, разрыв связей между кремнекислородными тетраэдрами и частичное повышение координационного числа ионов алюминия, образование из свободных оксидов муллита и кристобалита. Предложенный подход контролирует соотношение фаз Аl2О3 и SiO2 на определенных этапах, что в дальнейшем позволит улучшить механические и другие свойства матрицы получаемого сырья для целевых прототипов промышленных продуктов.
Отсутствует
Введение
Каолинит и другие глинистые минералы широко применяются в различных областях промышленности (атомной энергетике – в качестве основного компонента инженерных барьерных систем при захоронении радиоактивных отходов; строительстве; при производстве керамических изделий и огнеупоров и др.) благодаря своим высоким сорбционным свойствам и низкой водопроницаемости [1-3]. В качестве каолинитового сырья обычно используют природные каолины, что значительно сокращает расходы при производстве. Основным недостатком природного сырья является наличие примесей, влияющих на ход технологических процессов [4, 5] и качество целевого продукта [6-8]. В настоящее время в рамках мировых трендов и технологических вызовов, в том числе в области производства высокотехнологичных керамик и нанокомпозитов, принципиален поиск новых подходов к чистоте и составу исходного сырья [9-10] и моделированию физико-химических свойств целевых прототипов для различных индустриальных приложений [11-13].
Одним из наиболее интересных прототипов для промышленности является муллит (Al8[(O,OH,F)|(Si,Al)O4]4) (алюмосиликат) и самое высокотемпературное соединение – Al2O3 cSiO2, которое образуется при нагревании каолинита и других алюмосиликатов [14-16], приобретая разнообразные физико-химические и технические свойства, такие как низкие тепловое расширение и теплопроводность, высокое сопротивление ползучести, высокотемпературная прочность ихорошая химическая устойчивость [17-19]. Основной трудностью, связанной с получением муллита, является необходимость высоких температур, которые в зависимости от используемых методов и подходов отличаются на несколько сотен градусов. Поэтому актуальным остается вопрос поиска новых эффективных подходов получения муллитсодержащего сырья (а также композиционных материалов на его основе) из новых и альтернативных видов с целью получения заданного вещества при пониженных температурах.
Согласно истории проблемы, переход от метастабильной высокоглиноземистой фазы к термодинамически стабильной фазе муллита 3:2 является непрерывным процессом, включающим непрерывный твердый раствор между двумя формами муллита. В ходе экспериментальных работ выявлен фазовый переход первого порядка между двумя различными муллитами [20-22]. Таким образом, детальное изучение фазовых трансформаций каолинита при нагреве с учетом термодинамики процесса может улучшать механические и другие свойства получаемой матрицы. Кроме того, существующие ТУ (ТУ 1569-00396495489-05, ТУ 14-8-447-83) и промышленные стандарты предприятий для высокоглиноземистого мулитового сырья определяют необходимость контроля соотношения фаз Аl2О3 и SiO2, так как этот параметр является определяющим в дальнейшей утилизации полученного сырья.
Изучению алюмосиликатных систем посвящено много работ, поскольку именно эти системы лежат в основе большинства технологических процессов получения «умных» материалов (нанокомпозитов и нанореакторов) [23-25]. Для изучения реакций в алюмосиликатных системах Al-Si-O-Me все чаще используют математическое моделирование процессов [26-28] и термодинамический анализ [19, 20, 29] для последующего моделирования физико-химических свойств муллитового нанокомпозита в различных прикладных задачах.
Целью настоящей работы является получение муллита экспериментальным путем на основе каолинита Вежаю-Ворыквинского месторождения (соответствующего промышленным требованиям и ТУ) с учетом термодинамики алюмосиликатной системы. Для этого изучены структурные преобразования каолинита (системы Al-Si-O-Me), трансформации минеральных фаз, их физико-химических свойств в зависимости от термодинамики процесса.
Материалы и методы исследования
Образцы каолинита (Вежаю-Ворыквинское месторождение, Княжпогостcкий район, Республика Коми, 64°18'40.3"N, 51°08'31.5"E) были растерты до фракции –0,1мм (лабораторный дисковый истиратель ЛДИ-65). Термическую обработку образцов в интервале температур 570-1470К проводили в атмосфере печи трубчатой Carbolite Gero TF1 16/60/300, скорость нагрева 10К/мин, время выдержки 2ч. Морфология образцов каолинита (алюмосиликатных систем Аl2O3-SiO2) исследована с помощью сканирующей электронной микроскопии (TESCAN Vega 3). Фазовый состав образцов определялся по дифрактограммам неориентированных образцов. Съемка проводилась на рентгеновском дифрактометре Shimadzu XRD-6000, излучение CuKα, Ni-фильтр, 30 kV, 20 mA, область сканирования 2-65° 2θ. Содержание фаз оценивалось методом Ритвельда (программа Profex). Химический состав был определен рентгенофлуоресцентным методом (Shimadzu XRF-1800). ИК-спектры получены на Фурье-спектрометре ИнфраЛЮМ ФТ-02 в диапазоне 400-4000 см–1 (таблетки KBr 1000:1,7мг). Термогравиметрический анализ проведен с помощью Mettler Toledo TGA/DSC 3+ (интервал температур 300-1270К, скорость нагрева 10К/мин).
Результаты и обсуждение
Изучение вещественного состава исходного каолинитового сырья
Проведен комплексный анализ химического состава и соотношения фаз Al2O3/SiO2 в образцах каолинита до проведения экспериментов, % по массе: SiO2 51,41; Al2O3 43,79; TiO2 1,83; Fe2O3 1,53; K2O 0,43; CaO 0,38; MgO 0,33. Весовое отношение Al2O3/SiO2 составляет 0,852, что очень близко к теоретическому значению 0,85 для каолинита.
Рентгенофазовый анализ (РФА) показал, что исходный образец представлен каолинитом (~98%), присутствуют незначительные примеси диаспора и рутила (рис.1). На дифрактограммах исходного каолинита (рис.2) межплоскостное расстояние несколько больше идеального и составляет 7,2Å, а интенсивность рефлекса снижена, что позволяет предполагать существование некоторого количества межслоевой воды между силикатными слоями.
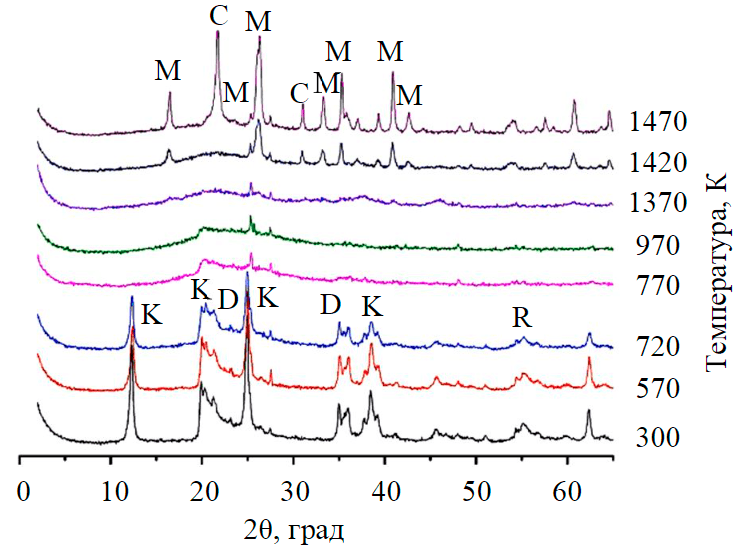
Рис.1. Дифрактограмма образцов каолинита исходного и отожженных при различной температуре K – каолинит; D – диаспор; R – рутил; M – муллит; C – кристобалит
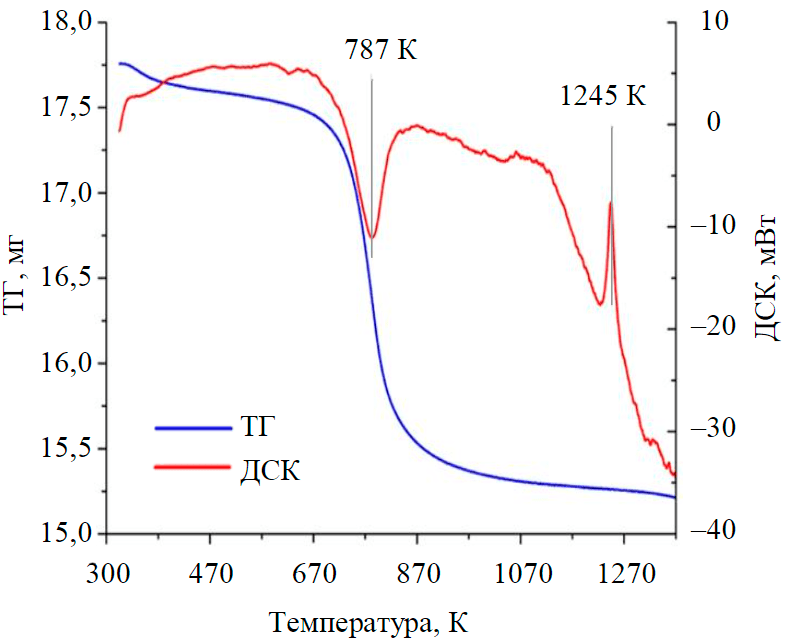
Рис.2. Кривые ТГ и ДСК образцов каолинита
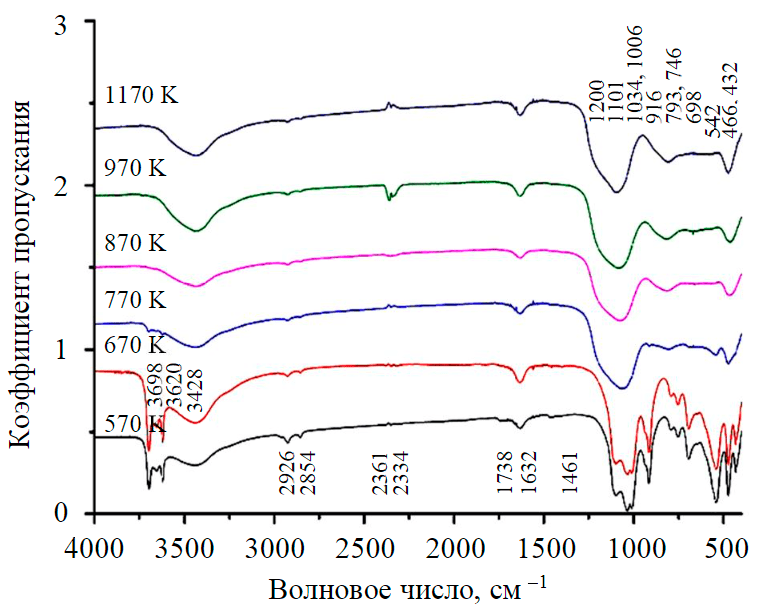
Рис.3. ИК-спектры образцов каолинита, обработанных при различной температуре
Экспериментальные исследования
При термической обработке каолинита в температурном интервале до 720К его структура практически не претерпевает изменений (рис.1).
При температуре 770-820 К наблюдается эндотермический эффект (рис.2), который на основании данных ИК-спектроскопии (рис.3) связывается с удалением гидроксильных групп, при этом в конце процесса алюмокислородный октаэдрический слой практически полностью перестаивается в алюмокислородный тетраэдрический образующейся промежуточной рентгеноаморфной фазы (метакаолинит), связь между слоями которого, вероятно, осуществляется через ионы кислорода, общие для алюмо- и кремнекислородного слоев (связь Si-O-Al) [9, 10]. На дифрактограммах эта неупорядоченная фаза характеризуется диффузными рефлексами (d/n~4,4; 2,5; 1,7Å), полностью исчезают базальные пики каолинита {001} – периодичность вдоль оси с. Пики {–110} и {020} (2q=20-25°) – параметры осей а и b – постепенно сглаживаются и полностью исчезают при достижении 1270К. С 1340К появляется еще одна промежуточная неидентифицируемая фаза с диффузными рефлексами (d/n~4,0-3,9; 2,0-1,9Å). При дальнейшем повышении температуры рефлексы этих фаз становятся более отчетливыми, а их межплоскостные расстояния меняются (d/n~ 4,2; 2,5; 2,0Å и псевдомуллит сd/n~ 4,0-3,9; 2,4; 1,9Å соответственно).
На кривой ДСК (рис.2) экзотермический эффект в интервале 1220-1270К объясняется, по всей видимости, окончательным разрушением кристаллической решетки каолинита, возможным распадом метакаолинита на свободные оксиды, разрывом связей между кремнекислородными тетраэдрами и частичным повышением координационного числа ионов алюминия.
Образование муллита фиксируется при температуре 1470К, на дифрактограмме появляются характерные дифракционные пики. Кристаллическая структура муллита состоит из спаренных цепочек Si2O5, в которых ион кремния частично изоморфно замещен ионом алюминия, который имеет как шестерную [АlO6], так и четверную [AlO4] координацию. При этой же температуре (1470К) фиксируется появление фазы кристобалита, образование которого происходит из-за избытка несвязанного кремнезема (в муллите соотношение 3, тогда как в исходном каолините Al/Si=2).

Рис.4. СЭМ-изображения исходного каолинита и отожженного при разных температурах
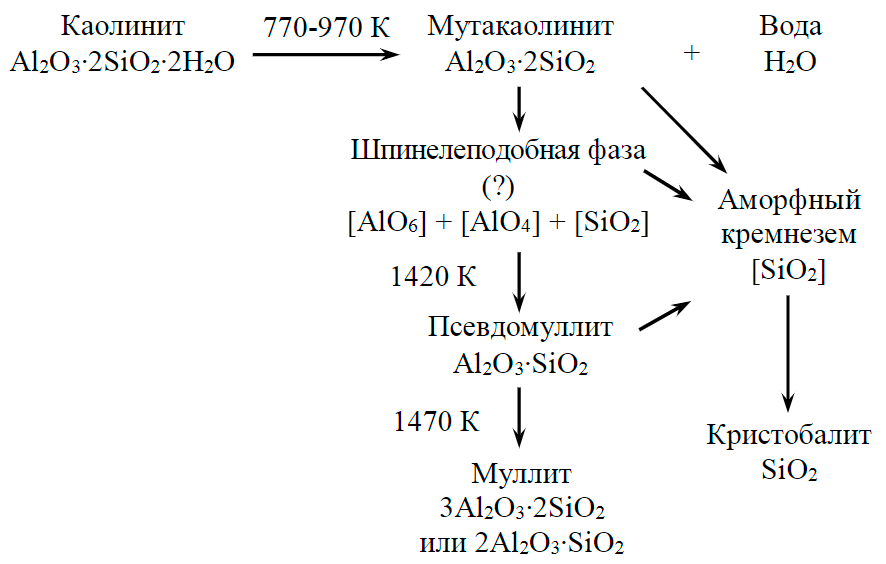
Рис.5. Блок-схема химических реакций твердофазного преобразования каолинита в муллит
ИК-спектроскопия
ИК-спектры исходного каолинита и отожженных образцов показаны на рис.3. Характерный пик поглощения при 1101см–1 был отнесен к валентным колебаниям Si-O-Si прокаленного каолинита, пик 916см–1 – к валентным колебаниям Al-O в четверной [AlO4] координации, а пик 575см–1 – к деформационным колебаниям Al-O в шестерной координации [АlO6] [30]. Пик 793см–1, формирующийся в свыше 770К, был отнесен к связи Si-O в кристобалите, характерный пик поглощения 466см–1 – к деформационным колебаниям Si-O. Пики 746см–1 и542см–1 относятся к образованию шпинелеподобной фазы [31]. Слабовыраженный пик 1200см–1, интенсивность которого убывает с увеличением температуры выдержки, связывается аморфным кремнеземом (метакаолинитом). ИК-спектры каолинита после температурной обработки согласуются с результатами РФА.
Электронная микроскопия
Последовательность этих фазовых трансформаций прослеживается на СЭМ: при повышении температуры происходит явная сегрегация зерен каолинита, образование более крупных по размеру агрегатов и четко видны элементы его перекристаллизации (рис.4). При повышении температуры до 1420 К на поверхности каолинита появляются короткие игольчатые кристаллы псевдомуллита. При 1470 К поверхность спекшихся частиц каолинита покрыта игольчатыми кристаллами псевдомуллита и хаотично расположенными зернами кристобалита. Приведенные данные РФА, ИК-спектроскопии и СЭМ хорошо согласуются с имеющимися литературными данными [21, 32].
Кинетический анализ кристаллизации муллита и кристобалита из каолинита
Данные о кинетике кристаллизации муллита и кристобалита из каолинита приведены в работе [29]. На основе представленных данных рентгенофазового анализа и ИК-спектроскопии процесс твердофазного образования муллита из каолинита представлен на рис.5.
На основе экспериментальных данных термодинамический процесс преобразования каолинита может быть представлен в виде следующих теоретических реакций:
А12O3∙2SiO2∙2Н2O ⇒ А12O3∙2SiO2+2Н2O;
Каолинит Метакаолинит
2(Al2O3∙2SiO2) ⇒ 2А12О3∙3SiO2+SiO2;
Метакаолинит Шпинель(?)
2А12О3∙3SiO2 ⇒ 2(А12О3∙SiO2)+SiO2;
Шпинель(?) Псевдомуллит
3(Al2О3∙SiO2) ⇒ 3А12O3∙2SiO2+SiO2; (1)
Псевдомуллит Муллит Кристобалит
2(Al2О3∙SiO2) ⇒ 2А12O3∙SiO2+SiO2. (2)
Псевдомуллит Муллит Кристобалит
Суммарная реакция:
3(А12O3 ∙ 2SiO2 ∙ 2Н2O) ⇒ 3А12О3 ∙ 2SiO2 + 4SiO2 +6H2O; (3)
2(А12O3 ∙ 2SiO2 ∙ 2Н2O) ⇒ 2А12О3 ∙ SiO2 + 3SiO2 +4H2O. (4)
Учитывая неустойчивость химического состава муллита (от 3Al2O3∙2SiO2 до 2Al2O3∙SiO2), предложены две реакции его образования из псевдомуллита (1) и (2), что, соответственно, находит отражение и в суммарных реакциях (3) и (4).
Приведенные реакции являются чистыми. В реакциях с участием исходных образцов присутствуют различные примеси окислов железа, титана и т.д. Предполагая, что в первом приближении примеси не оказывают влияния на получение конечных продуктов, используем эти реакции для расчета энергии Гиббса (изобарного потенциала) при различных температурах. Какая из реакций будет более предпочтительной в энергетическом отношении, определяется величиной изменения энергии Гиббса в ходе реакции [33].
Для расчета изменения энергии Гиббса используется термодинамическое соотношение Гиббса – Гельмгольца, связывающее энтальпию H с энергией Гиббса G [34]:
Интегрируя это соотношение, приведем его к такому виду:
где G1 – энергия Гиббса при температуре T1; как правило, в качестве T1 берется температура T = 298 К, тогда вместо константы интегрирования G1 записывается ΔG0298, а вместо G и H – изменения этих величин: ΔG – изменение энергии Гиббса в ходе реакции, DH – изменение теплоты образования веществ.
Тогда формула (5) примет вид:
Для вычисления по формуле (6) необходимо знать зависимость энтальпии от температуры, которая определяется по следующей формуле:
где Cp(Т) – зависимость теплоемкости от температуры, вычисляемая интерполяционной формулой
Константы a, b, c, ΔH0298, ΔG0298 для веществ, входящих в реакции, берутся из справочных таблиц (Карапетьянц М.Х. Химическая термодинамика. М.: Либроком, 2019. 584 с). Для каждой отдельной реакции константы вычисляются по следующим формулам:
где vi, vj – стехиометрические коэффициенты.
Изменение энергии Гиббса в зависимости от температуры для реакций (3) и (4) представлены на рис.6. Согласно термодинамике, система при постоянных температуре и давлении обладает в равновесном состоянии наименьшей энергией Гиббса. Кривая ΔG(Т) для реакции (3) при любой температуре идет ниже, т.е. с термодинамической точки зрения является предпочтительной.
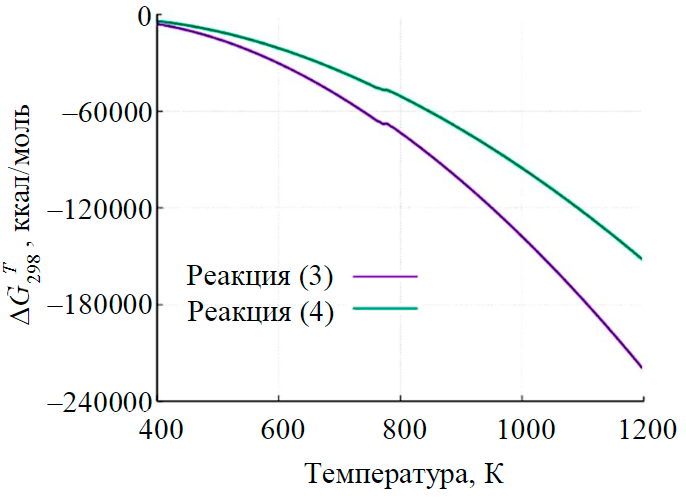
Рис.6. Изменение энергии Гиббса в зависимости от температуры
Выводы
Впервые муллит получен экспериментальным путем на основе каолинита Вежаю-Ворыквинского месторождения с учетом термодинамики алюмосиликатной системы.
Проведено экспериментальное исследование фазовой трансформации каолинита при термической обработке в интервале температур 670-1470К. Показано, что образование целевого продукта – муллитового нанокомпозита – протекает в несколько фаз: метаколинит, вода, шпинелеобразная фаза, аморфный кремнезем, псевдомуллит.
Муллитовая фаза фиксируется при температуре 1470К с появлением кристобалита. Образование кристобалита происходит из-за избытка несвязанного кремнезема (в муллите Al/Si=3, тогда как в исходном каолините Al/Si=2).
Преобразования структуры исходного каолинита включают удаление структурной воды с разделением кремнекислородного тетраэдрического и алюмокислородного октаэдрического слоев, распад на свободные оксиды, разрыв связей между кремнекислородными тетраэдрами и частичное повышение координационного числа ионов алюминия, образование из свободных оксидов муллита и кристобалита.
На основе анализа термодинамики химических реакций определен менее энергозатратный тип реакции для получения мулитосодержащего нанокомпозита. Предложенный подход контролирует соотношение фаз Аl2О3 и SiO2 на определенных этапах, что в дальнейшем позволит улучшить механические и другие свойства матрицы получаемого сырья для целевых прототипов промышленных продуктов.
Литература
- Pusch R., Knutsson S., Al-Taie L., Mohammed M.H. Optimal ways of disposal of highly radioactive waste // Natural Science. 2012. Vol. 4. Special Issue. P. 906-918. DOI: 10.4236/NS.2012.431118
- Sellin P., Leupin O.X. The use of clay as an engineered barrier in radioactive-waste management – a review // Clay Minerals. 2013. Vol. 61. Iss. 6. P. 477-498. DOI: 10.1346/CCMN.2013.0610601
- Biswal B., Mishra D.K., Das S.N., Bhuyan S. Structural, micro-structural, optical and dielectric behavior of mullite ceramics // Ceramics International. 2021. Vol. 47. Iss. 22. P. 32252-32263. DOI: 10.1016/j.ceramint.2021.08.120
- Евтушенко Е.И., Сыса О.К., Ляшенко О.В., Новоселов А.Г. Комплексный анализ структурных изменений гидротермально-стабилизированных каолинов // Вестник Белгородского государственного технологического университета им. В.Г.Шухова. 2012. № 3. C. 150-154.
- Cui K., Zhang Y., Fu T. et al. Toughening Mechanism of Mullite Matrix Composites: A Review // THE Coatings. 2020. Vol. 10. P. 672-696. DOI: 10.3390/coatings10070672
- Салахов А.М., Салахова Р.А., Ильичева О.М. и др. Влияние структуры материалов на свойства керамики // Вестник Казанского технологического университета. 2010. № 8. С. 343-349.
- Al-Shantir O., Trník A., Csáki Š. Influence of firing temperature and compacting pressure on density and Young’s modulus of electroporcelain // AIP Conference Proceedings. 2018. № 1988. DOI: 10.1063/1.5047595
- De Aza A.H., Turrillas X., Rodriguez M.A. et al. Time-resolved powder neutron diffraction study of the phase transformation sequence of kaolinite to mullite // Journal of the European Ceramic Society. 2014. Vol. 34. Iss. 5. P. 1409-1421. DOI: 10.1016/j.jeurceramsoc.2013.10.034
- Kotova O.B., Ignatiev G.V., Shushkov D.A. et al. Preparation and Properties of Ceramic Materials from Coal Fly Ash /Minerals: Structure, Properties, Methods of InvestigationSpringer.Proceedings in Earth and Environmental Sciences. Springer, Cham, 2019. P. 100-107. DOI: 10.1007/978-3-030-00925-0_16
- Tong L.X., Li J.H., Liu F. Preparation of Mullite Nanocomposites Powders by the Hydrothermal Crystallization Method from Coal Gangue // Key Engineering Materials. 2012. Vol. 512-515. P. 49-53. DOI: 10.4028/www.scientific.net/KEM.512-515.49
- Chandrasekhar S., Ramaswamy S. Influence of mineral impurities on the properties of kaolin and its thermally treated products // Applied Clay Science. 2002. Vol. 21. P. 133-142. DOI: 10.1016/S0169-1317(01)00083-7
- Glinchuk M.D., Bykov I.P., Kornienko S.M. et al. Influence of Impurities on the Properties of Rare-Earth-Doped Barium-Titanate // Journal of Materials Chemistry. 2000. Vol. 10. P. 941-947. DOI: 10.1039/A909647G
- Romero A.R., Elsayed H., Bernardo E. Highly porous mullite ceramics from engineered alkali activated suspensions // Journal of the American Ceramic Society. 2018. Vol. 101. P. 1036-1041. DOI: 10.1111/JACE.15327
- Bai J. Fabrication and properties of porous mullite ceramics from calcined carbonaceous kaolin and α-Al2O3 // Ceramica International. 2010. Vol. 36. Iss. 2. P. 673-678. DOI: 10.1016/J.CERAMINT.2009.10.006
- Gustafsson S., Falk L.K., Pitchford J.E. et al. Development of Microstructure during Creep of Mullite and Mullite 5 vol% SiC Nanocomposite // Journal of the European Ceramic Society. 2009. Vol. 29. Iss. 4. P. 539-550. DOI: 10.1016/j.jeurceramsoc.2008.06.036
- Lisuzzo L., Cavallaro G.P., Milioto S., Lazzara G. Halloysite nanotubes as nanoreactors for heterogeneous micellar catalysis // Journal of Colloid and Interface Science. 2021. № 608. P. 424-434. DOI: 10.1016/j.jcis.2021.09.146
- Ситева О.С., Медведева Н.А., Середин В.В. и др. Влияние давления на структуру каолинита в огнеупорных глинах Нижне-Увельского месторождения по данным ИК-спектроскопии // Известия Томского политехнического университета. Инжиниринг георесурсов. 2020. Т. 331. № 6. С. 208-217. DOI: 10.18799/24131830/2020/6/2690
- Botero C.A., Jimenez-Piqué E., Martín R. et al. Nanoindentation and Nanoscratch Properties of Mullite-Based Environmental Barrier Coatings: Influence of Chemical Composition-Al/Si Ratio // Surface and Coatings Technology. 2014. Vol. 239. P. 49-57. DOI: 10.1016/j.surfcoat.2013.11.016
- Zhou H.M., Qiao X.C., Yu J.G. Influences of quartz and muscovite on the formation of mullite from kaolinite // Applied Clay Science. 2013. Vol. 80-81. P. 176-181. DOI: 10.1016/J.CLAY.2013.04.004
- Жалилов А., Эшбуриев Т. Термодинамический анализ образования муллита из каолинита // Universum: химия и биология. 2021. № 5 (83). C. 51-54.
- Ламберов А.А., Ситникова Е.Ю., Абдулганеева А.Ш. Влияние состава и структуры каолиновых глин на условия перехода каолинита в метакаолинит // Вестник Казанского технологического университета. 2011. № 7. С. 17-23.
- Schmücker M., Schneider H., MacKenzie K.J.D. et al. AlO4/SiO4 distribution in tetrahedral double chains of mullite // Journal of the American Ceramic Society. 2005. Vol. 88. Iss. 10. P. 2935-2937. DOI: 10.1111/J.1551-2916.2005.00500.X
- Абдрахимов В.З., Колпаков А.В., Денисов Д.Ю. Кристаллизация муллита при синтезе керамических материалов из отходов производств // Концепт. 2013. Т. 3. С. 2716-2720.
- Bartsch M., Saruhan B., Schmücker M., Schneider H. Novel Low-Temperature Processing Route of Dense Mullite Ceramics by Reaction Sintering of Amorphous SiO2-Coated -Al2O3 Particle Nanocomposites // Journal of the American Ceramic Society. 2004. Vol. 82. № 6. P. 1388-1392. DOI: 10.1111/J.1151-2916.1999.TB01928.X
- Sarkar R., Mallick M. Formation and densification of mullite through solid-oxide reaction technique using commercial-grade raw materials // Bulletin of Materials Science. 2018. Vol. 41. P. 1-8. DOI: 10.1007/s12034-017-1533-7
- Дубовиков О.А., Николаева Н.В. Математическое описание процесса разложения каолинита щелочными растворами // Записки Горного института. 2011. Т. 192. С. 73-76.
- Sperinck S., Raiteri P., Marks N., Wright K. Dehydroxylation of Kaolinite to Metakaolin – A Molecular Dynamics Study // Journal of Materials Chemistry. 2011. Vol. 21. Iss. 7. P. 2118-2125. DOI: 10.1039/C0JM01748E
- Zhou Y., Liu Q., Xu P. et al. Molecular Structure and Decomposition Kinetics of Kaolinite/Alkylamine Intercalation Compounds // Frontiers in Chemistry. 2018. Vol. 6. № 310. DOI: 10.3389/fchem.2018.00310
- Ondro T., Al-Shantir O., Csáki S. et al. Kinetic analysis of sinter-crystallization of mullite and cristobalite from kaolinite // Thermochimica Acta. 2019. Vol. 678. № 1783121. DOI: 10.1016/J.TCA.2019.178312
- Дятлова Е.М., Бобкова Н.М., Сергиевич О.А. ИК-спектроскопическое исследование каолинового сырья белорусских месторождений // Проблемы недропользования. 2019. № 2 (21). C. 143-149. DOI: 10.25635/2313-1586.2019.02.143
- Weiquan Yuan, Jingzhong Kuang, Zheyu Huang, MingmingYu. Effect of aluminum source on the kinetics and mechanism of mullite preparation from kaolinite // Chemical Physics Letters. 2022. Vol. 787. № 139242. DOI: 10.1016/j.cplett.2021.139242
- Lee S., Kim Y., Moon H.-S. Phase Transformation Sequence from Kaolinite to Mullite Investigated by an Energy-Filtering Transmission Electron Microscope // Journal of the American Ceramic Society. 2004. Vol. 82. P. 2841-2848. DOI: 10.1111/J.1151-2916.1999.TB02165.X
- Gmehling J., Kleiber M., Kolbe B.D., Rarey J. Chemical Thermodynamics for Process Simulation. Wiley-VCH, 2019. 805 p.
- Fegley B. Practical Chemical Thermodynamics for Geoscientists. Elsevier, 2013. 813 p. DOI: 10.1016/C2009-0-22615-8
